Våra projekt
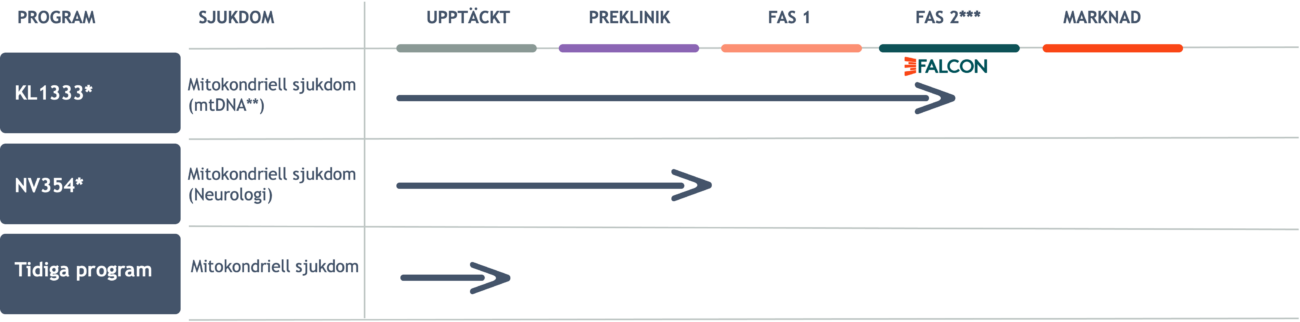
**mtDNA-relaterade mitokondriella sjukdomar som orsakas av mutation(er) i mitokodriellt DNA (till skillnad från nukleärt DNA).
***Eftersom mitokondriella sjukdomar är sällsynta sjukdomar har en fas 2-studie i dessa patienter, om den lyckas, potential att betraktas som registreringsgrundande.
KL1333: Innovativ läkemedelskandidat i sen utvecklingsfas
Projektstatus: Positiv interimsanalys av data från patienter i Steg 1 av FALCON-studien
FALCON är en global, randomiserad, placebokontrollerad och potentiellt registreringsgrundande fas 2-studie där säkerhet och effekt av KL1333 utvärderas hos vuxna patienter med primär mitokondriell sjukdom som upplever ihållande och svår trötthet/utmattning och myopati (muskelsvaghet), vilka är de vanligaste och mest begränsande symptomen.
Totalt 180 patienter med mutationer i det mitokondriella DNA:t som uppfyller inklusionskriterierna randomiseras 3:2 för att få KL1333 (50 mg-100 mg) eller placebo två gånger dagligen i 48 veckor. Genom de två alternativa primära effektmåtten bedöms ihållande trötthet/utmattning (med frågeformuläret PROMIS Fatigue Mitochondrial Disease) och muskelsvaghet (med 30 Second Sit-to-Stand-testet), varav endast ett måste vara positivt för ansökan om marknadsgodkännande.
I juni 2023 doserades den första patienten. En interimsanalys, vilken genomfördes i juli 2024, där 24-veckorsdata från patienterna i det första steget av studien utvärderades, bekräftade KL1333:s goda säkerhetsprofil, och båda effektmåtten klarade futilitetstestet, dvs båda har potential att kunna påvisa effekt i studiens slutliga analys.
KL1333 har särläkemedelsklassificering i både Europa och USA samt Fast Track-status i USA.
Patientpopoulation inom mitokondriella sjukdomar: MELAS-MIDD och KSS-CPEO och MERRF
Ablivas huvudkandidat KL1333 har utformats för att behandla ihållande trötthet och utmattning samt myopati (muskelsvaghet) hos vuxna patienter med en genetiskt bekräftad primär mitokondriell sjukdom. Diagnoser kan inbegripa sjukdomasspektrumen MELAS-MIDD och KSS-CPEO samt MERRF:s syndrom. Läkemedelskandidaten är avsedd för oral långtidsbehandling.
Verkningsmekanism: NAD⁺/NADH-modulering
KL1333 reglerar de cellulära nivåerna av NAD+ och NADH, centrala koenzymer i cellens energimetabolism. Denna reglering leder till bildandet av nya mitokondrier och förbättrade energinivåer på cellnivå, vilket förväntas leda till en förbättring på kroppsnivå av energi och organfunktion hos patienterna i FALCON-studien.
NV354: Banbrytande läkemedelsbehandling för stort medicinskt behov
Projektstatus: Preklinisk utveckling slutförd
Den prekliniska utvecklingen har slutförts, och läkemedelskandidaten har beviljats särläkemedelsklassificering både i EU och USA. Med tanke på prioriteringen av KL1333-programmet planeras inga kostnadskrävande operativa aktiviteter för NV354 för närvarande.
Patientpopoulation inom primära mitokondriella sjukdomar: Neurologi
NV354 utvecklas för mitokondriell sjukdom med neurologiska komplikationer, i synnerhet vid otillräcklig aktivitet i proteinkomplex I i mitokondrierna. Den resulterande dysfunktionen i energiomvandling ger upphov till kliniska tecken och symptom vid många typer av mitokondriell sjukdom, inklusive neurologiska komplikationer som ses vid Leighs syndrom, MELAS eller LHON. Det finns även utökade möjligheter utanför området mitokondriell sjukdom, till exempel vid neurologiska tillstånd där mitokondriell dysfunktion har bekräftats.
Läkemedelskandidaten upptäcktes på grund av dess förmåga att öka mitokondriell aktivitet i celler från patienter med det mitokondriella Leighs syndrom. Leighs syndrom debuterar vanligtvis vid ett till två års ålder och inbegriper psykomotorisk regression, hypotoni och utvecklingsförseningar. Sjukdomen är dödlig, och barn med tidigt debuterande Leighs syndrom dör oftast före vuxen ålder.
Verkningsmekanism: Energiersättning
NV354, som har god upptagsförmåga till hjärnan, bygger på en innovation där kroppens eget energisubstrat, succinat, görs tillgängligt i cellen via en prodrogteknologi. En prodrog är ett inaktivt läkemedel som aktiveras först när det kommer in i kroppen genom en omvandling av dess kemiska struktur.
Tidig utvecklingsfas
Abliva bedriver forskning för att identifiera ytterligare utvecklingsprogram med inriktning mot reglering och stabilisering av cellulär energiproduktion.